铸成
视角
第四次修订的《中华人民共和国专利法》(以下简称“专利法”)于2021年6月1日正式实施,标志着中国药品链接制度正式落地,截止撰文日,该制度实施已有四年多。本系列文章聚焦于中国药品专利链接制度,介绍制度立法和制度内容,并通过整理和分析相关案件数据,总结了制度实践中已经形成的审理规则,以供读者参考。
(一)什么是药品专利链接制度?
药品专利链接制度是指在药品上市审批过程中,将药品相关专利权状态与药品注册程序进行“链接”。通过制度设计,在仿制药获批前提前解决潜在的专利侵权争议,以兼顾仿制药上市效率与原研药专利权保护之间的平衡。
该制度要求仿制药申请人在提交上市申请时,就涉及的专利做出声明。如存在争议,原研药专利权人或利害关系人可以在审评阶段提起民事诉讼或行政裁决程序,要求判定仿制药是否落入其专利保护范围。药监部门则可在法院判决或行政裁决作出前,暂停审批该仿制药的上市许可。
(二)法律依据与制度建设
中国药品专利链接制度的法律基础来自2020年修订的《专利法》第七十六条。该条明确:在药品审评审批过程中,因申请药品涉及他人专利权产生纠纷的,当事人可以向法院提起诉讼,或向中国国家知识产权局(以下简称“国知局”)申请行政裁决。国务院药品监督管理部门(即国家药品监督管理局,以下简称“国药监局”)可根据法院生效判决决定是否暂停药品上市审批。
为落实专利法第七十六条,国药监局与国知局于2021年联合发布《药品专利纠纷早期解决机制实施办法(试行)》(以下简称“《实施办法》”),同时国知局发布《药品专利纠纷早期解决机制行政裁决办法》(以下简称“《裁决办法》”)为药品链接案件的处理提供指引。最高人民法院发布的《关于审理涉药品上市审评审批专利民事案件适用法律若干问题的规定》(以下简称“《药品专利民事案件司法解释》”)也是法院进行审理时的重要依据。
(三)案件受理情况
1. 行政裁决
截至2025年11月14日,国家知识产权局公开的药品专利行政裁决共183份。其中,超过一半(98件)的案件由请求人主动撤回。在作出实质裁决的案件中,有37件被认定落入专利保护范围,占比约20.2%;34件被认定未落入专利保护范围,占比约18.6%;14件因不符合法定条件被裁定驳回请求,占比约7.7%。
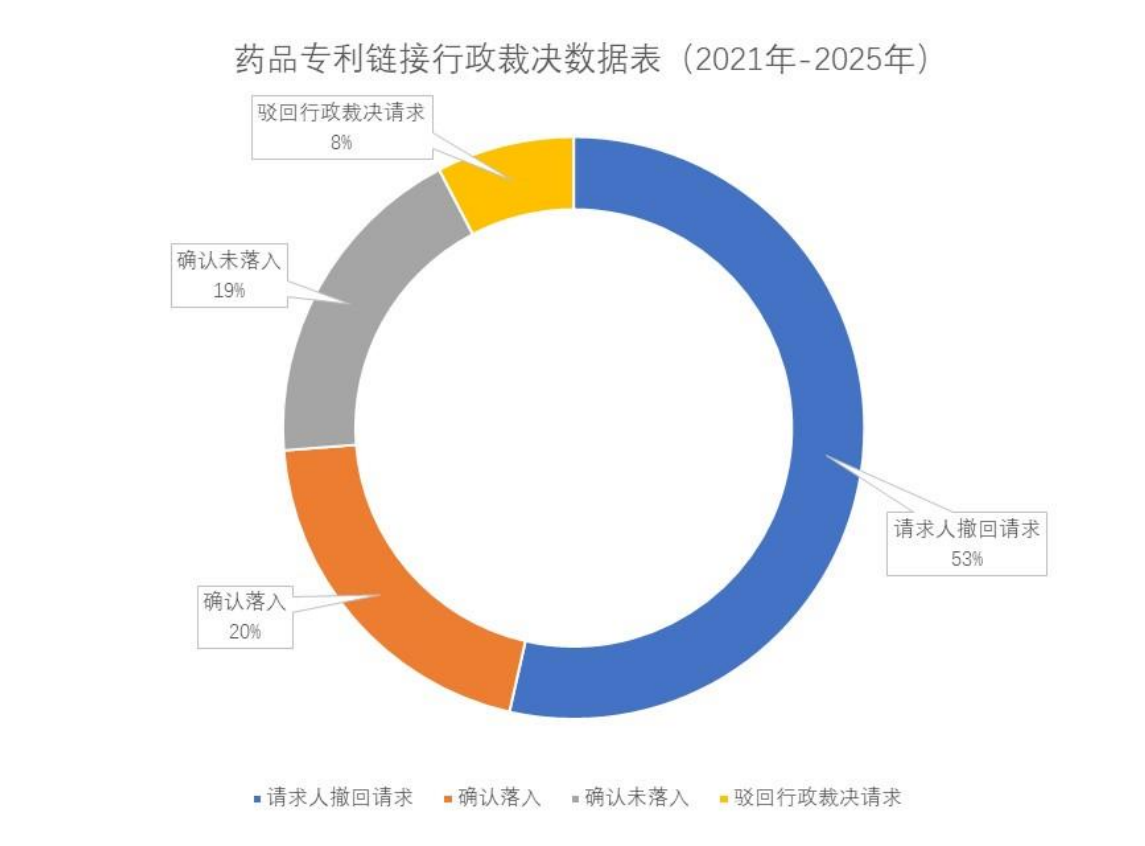
2. 民事判决与裁定
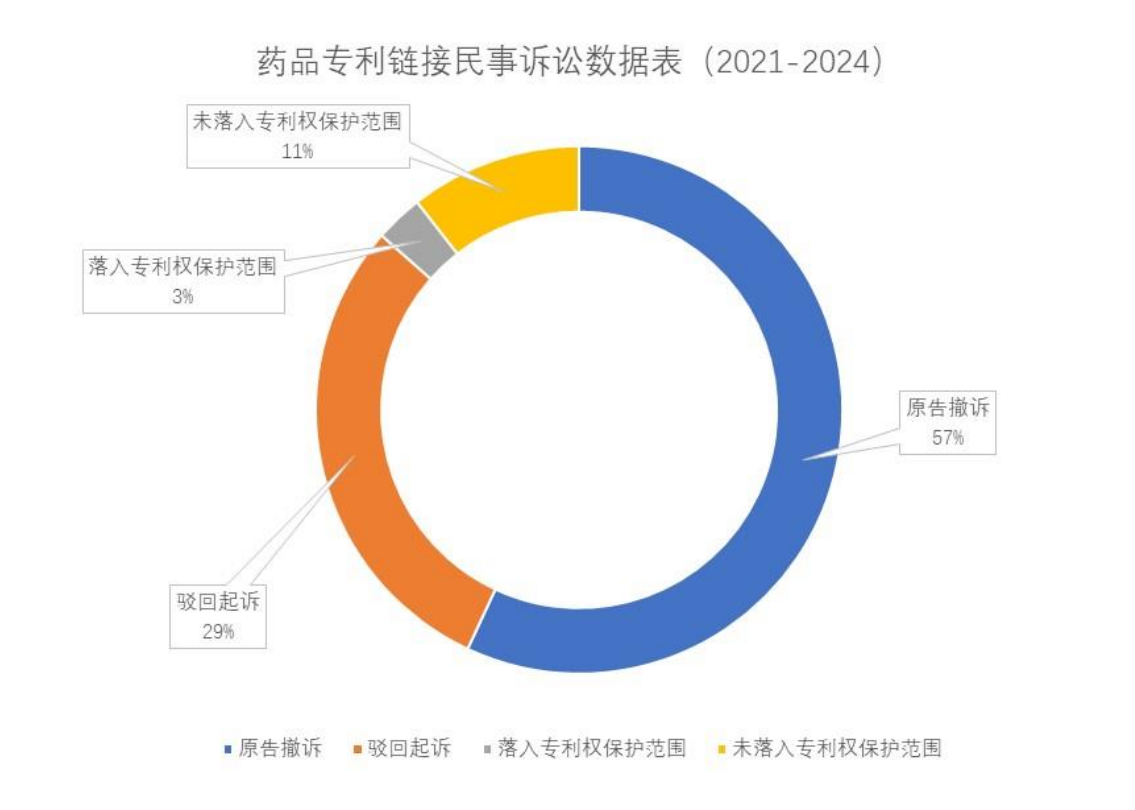
截至同日,裁判文书网及主要法律数据库共公开了50份与药品专利链接相关的民事裁判文书,其中一审案件32件,二审案件18件。约54%的案件中,原告在诉讼过程中主动撤诉,剩余案件中14件被驳回起诉,仅9件案件进入实体审理并最终获得法院判决。
(一)适用药品专利纠纷早期解决机制的条件
适用药品专利纠纷早期解决机制需要满足多个前提条件,根据《专利法》的相关规定,需满足下列条件:
进一步的,在案件实体审理过程中,还会涉及到下述具体问题:
药品上市许可持有人需在上市药品专利信息登记平台登记在中国境内注册上市的药品相关专利信息。其中,“相关专利信息”需要满足两个条件,一是需为已经在中国上市的原研药相对应地登记在专利信息登记平台的专利 ;二是原研药本身的技术方案需落入登记专利权利要求的保护范围之内 。此外,登记专利需在《实施办法》规定的可登记的专利类型范围内。
(二)药品专利纠纷早期解决机制的程序
1. 药品上市许可持有人进行专利信息登记
根据《实施办法》第四条的规定,适用药品专利纠纷早期解决机制首先需要上市许可持有人在获得药品注册证后30日内进行专利信息登记。如专利信息发生变更,上市许可持有人需在变更生效后30日内完成更新。
登记平台仅做形式审查,上市许可持有人需对所有信息的真实性、准确性以及完整性负责,同时所有登记信息需保持一致性,包括:
根据《实施办法》及其政策解读的相关规定,可登记/不可登记的专利类型如下:
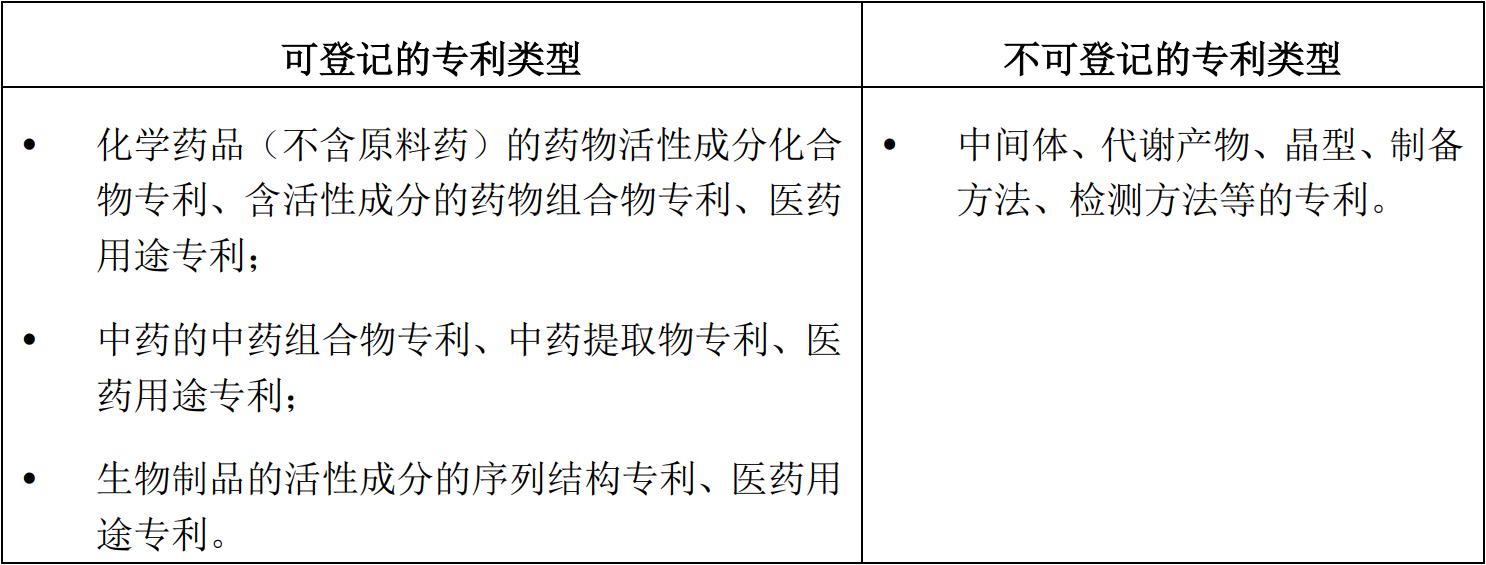
2. 仿制药申请人作出声明
《实施办法》第六条及第十二条规定,化学仿制药、中药同名同方药、生物类似药申请人应在提交药品上市许可申请时,对照已在中国上市药品专利信息登记平台公开的专利信息,针对被仿制药每一件相关的药品专利作出声明,具体如下:
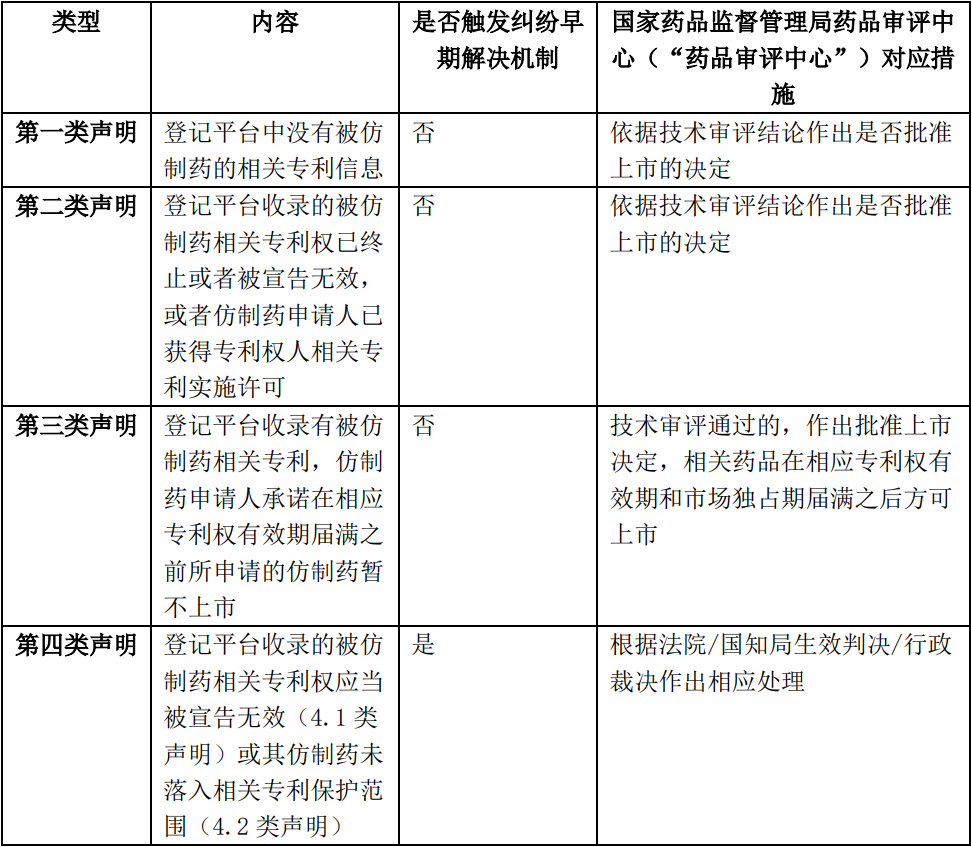
仿制药申请人作出声明后,国家药品审评机构(即药品审评中心)应在10个工作日内在信息平台向社会公开申请信息和相应声明。仿制药申请人应对相关声明的真实性、准确性负责,同时应将声明及其依据通知上市许可持有人,上市许可持有人非专利权人的,由上市许可持有人通知专利权人。如声明未落入相关专利权保护范围的,声明依据应当包括仿制药技术方案与相关专利的相关权利要求对比表及相关技术资料。
需注意,根据(2023) 国知药裁 0007号行政裁决,虽然国知局认定仿制药申请人怠于履行《实施办法》第六条规定的信息交换义务的行为具有可责性,但在信息交换义务的履行与仿制药技术方案是否落入专利权保护范围的判断也没有直接关联的情况下,责令被请求人履行信息交换义务的请求不能被纳入行政裁决的审理范围。根据该裁决,在行政裁决里请求仿制药申请人变更其声明类型或者履行向上市持有人通知声明及声明依据的诉讼请求可能不会被国知局支持。
3. 由专利权人或利害关系人/仿制药申请人启动纠纷早期解决民事诉讼/行政裁决程序
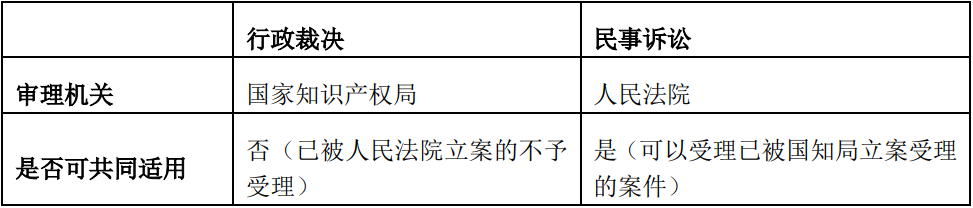
仿制药上市许可申请公开后,药品审评中心公开药品上市许可申请之日起45日内专利权人或利害关系人(即相关专利的被许可人或者登记的药品上市许可持有人)对四类声明有异议,可向人民法院提起诉讼或者向国家知识产权局请求行政裁决。同时,专利权人或者利害关系人在衔接办法规定的期限内(45日内)未向人民法院提起诉讼的,根据《药品专利民事案件司法解释》第四条,药品上市许可申请人(即仿制药申请人)可以向人民法院起诉或请求国知局对药品专利纠纷进行行政裁决,请求确认申请注册药品未落入相关专利权保护范围。
需要注意的是,《实施办法》里明确规定了国家知识产权局受理药品专利纠纷行政裁决的条件之一是人民法院此前未就该药品专利纠纷立案,而《药品专利民事案件司法解释》则规定了,当事人以国务院专利行政部门已经受理专利法第七十六条所称行政裁决请求为由,主张不应当受理专利法第七十六条所称诉讼或者申请中止诉讼的,人民法院不予支持。
收到当事人提交的人民法院立案或者国知局受理通知书副本后,国务院药品监督管理部门(即国药监局)对化学仿制药注册申请设置 9 个月的等待期。等待期自法院立案或者国知局受理之日起,只设置一次。等待期内国家药品审评机构(即药品审评中心)不停止技术审评。根据国知局或法院的处理结果,药品审评中心将作不同的处理:
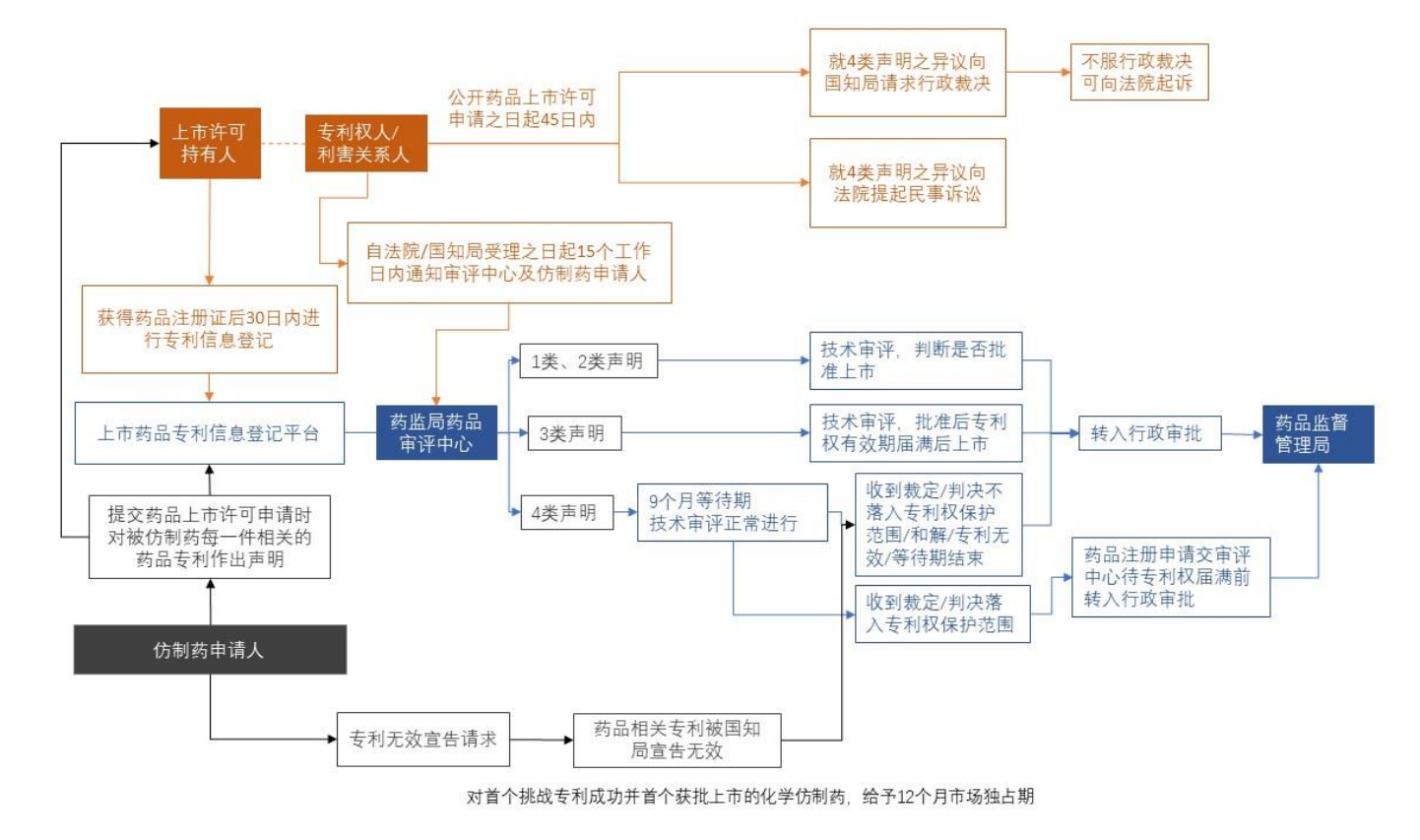
中药同名同方药和生物类似药注册申请不设等待期,审评中心将直接作出是否批准上市的决定,如法院或国知局确认相关技术方案落入相关专利保护范围的,相关仿制药在相应专利有效期届满后方可上市。
以上为药品专利链接制度的概况、适用条件以及基本程序的概括性介绍。关于药品专利链接案件的具体受理条件、举证责任和其他相关实务问题,我们将在下一篇文章中作进一步探讨。